生物学新纪元——基因编辑简史
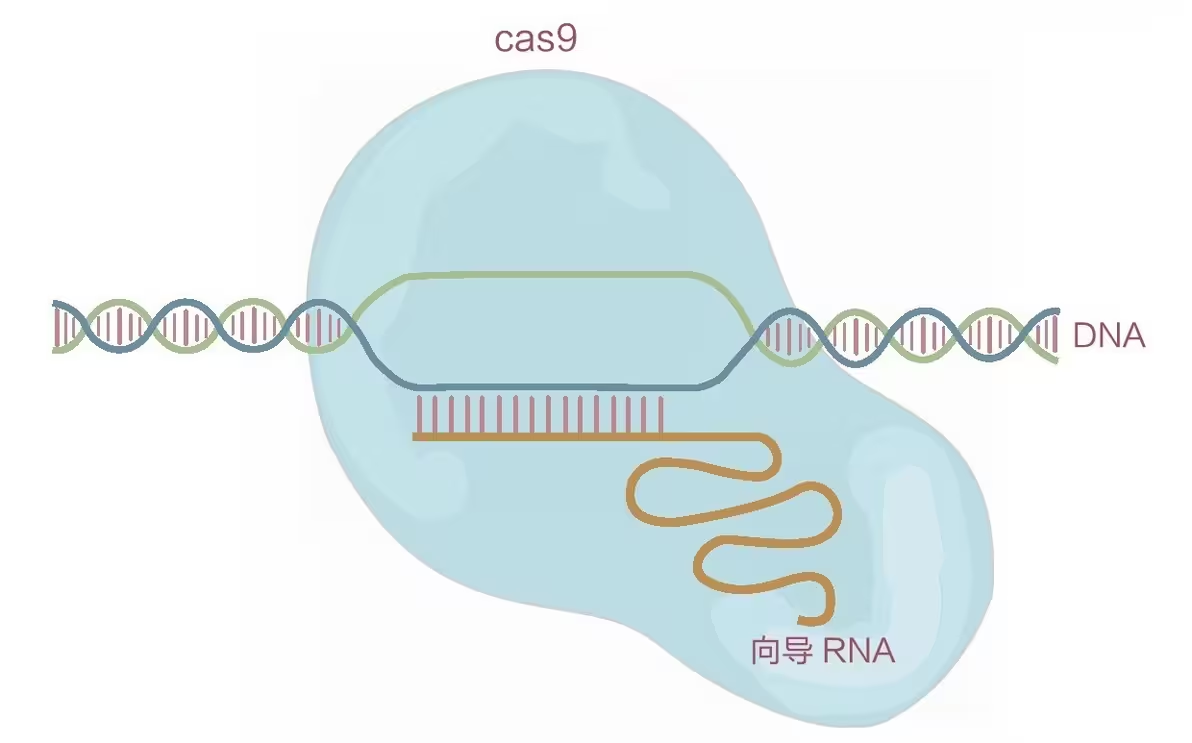
随后,向导RNA与CRISPR associate protein(Cas蛋白)也被发现。2014年,Jennifer,一位美国的生物化学家,首先阐明了CRISPR/Cas9系统的工作原理,证明它可以根据一段向导RNA的指引,找到对应的DNA序列,并将其切开。同时,他们还开发出了根据CRISPR系统来精准编辑目的基因的技术。随后不久,MIT的华人生物学家张锋又证明了这一系统同样可以在包括人在内的哺乳动物细胞中使用。自此,一个以CRISPR为主角的全新的基因编辑时代到来了。
为什么CRISPR这两年的发展会如此迅猛,甚至到达了ZFP和TALE当年完全不能企及的高度呢?关键还是在于CRISPR的便利性。还记得我们做的计算吗?ZFP和TALE需要用成百上千个碱基的长度来完成定位系统的组装,而CRISPR则只需要与目的基因一一对应的一段向导RNA即可完成这个任务,将基因定位的工作的工作量一下子削减到了原来的1/100。
CRISPR/Cas系统的另一个优势在于,Cas9蛋白自己本身就具有核酸内切酶的活性,而非ZFP和TALE那样只能定位到目的DNA上,得要另外结合一个核酸内切酶才能组成一个完整的基因编辑工具。
当然CRISPR也有着不小的缺点,最常为人称道的莫过于脱靶效应。这是由于CRISPR原本作为免疫系统的一部分,它的靶基因是病毒的DNA序列,因此为了防止病毒出现一些细微的变异,即使目的基因与向导RNA存在几个碱基的差异,它依然会毫不犹豫地将其切断。也就是说,一段与你目标DNA序列相似但无关的序列,也有可能会被切断并产生基因突变,而这无疑是生物学家不想看到的。CRISPR的另一个限制在于它对PAM序列的要求,目标DNA的最后几个碱基并不是与向导RNA结合,而是与Cas蛋白结合,因此结合序列的最后几个碱基是必须完全符合,而非可以自由选择的。例如Cas9的PAM就是NGG,N代表任意碱基,只有目的基因能够符合PAM序列的情况下,Cas9蛋白才能与它有效结合并进行切割,否则DNA切割率便会十分低(但并不是完全没有)。
另外还有一些CRISPR有可能触发机体免疫反应的担忧,但是这些困难并不足以使生物学家对CRISPR和基因编辑的热情减少一丝一毫,各种改良版的CRISPR和以CRISPR为基础的各种技术如今依然在以相当快的节奏不断涌出。一个宏伟的大基因编辑时代已然到来。
我在文章开头就试图传达这样一个概念,基因编辑技术是从DNA定位系统发展而来的,而当我们有了DNA定位系统,可以做到的事情显然不仅限于基因编辑。如果说基因编辑只是暴力地在DNA上切开一道口子,然后让其自生自灭,寄希望于引入一个随机突变的话,基于DNA定位系统的其他工具则更类似对DNA进行精细的手术。
前文中也已提到,CRISPR/Cas9系统是一个自带核酸内切酶的工具,但是我们完全可以通过蛋白质工程的手段,将Cas9蛋白的酶切位点失活,然后再连上一个具有其他功能的蛋白,我们就可以对特定DNA序列进行一些精细的操作。例如对单个碱基的修改,或者是对表观遗传修饰的修改(无论是DNA甲基化还是组蛋白修饰)。
除此之外,Cas9蛋白只是与CRISPR序列一起发挥作用的蛋白之一,另外还有许多其他的Cas蛋白,它们各自拥有非常独特的特性,比如Cas13可以切割靶向的RNA,Cas12a则可以切割单链的DNA。CRISPR技术的两位奠基人,Jennifer和张锋分别基于这两种蛋白的特性,开发出了被称为DETECTR和SHERLOCK的两种新技术,可以用来检测血液中的游离DNA,从而快速筛查特定病毒的感染情况。
具体的工作原理感兴趣的可以自己去查,我写到这里已经懒得再继续下去了……
简单总结一下,从ZFN开始,生物学家对好用的DNA定位系统的追寻从未停止过,基因编辑技术自然是最重要的目的之一,另一方面,DNA定位系统与其他生物酶的结合使我们可以对DNA进行更多更精细的操作,这也是CRISPR系统的一个重要发展方向。好的,那么我们下次见啦~
ps. 写在最后。做基因编辑也要遵守基本法,比如生殖系细胞(包括精子卵子受精卵)就不能随便编辑,如果编辑了,也绝对不能在体外培养超过14天,更不用说植入子宫让其发育到出生了。(生物学领域的国际惯例这样规定)
发表回复